เนื้อหา
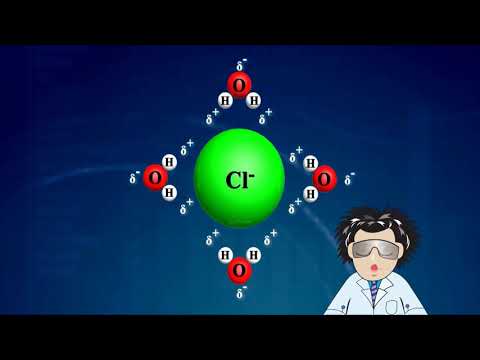
การค้นหาว่าสารประกอบนั้นเป็นอิเล็กโทรไลต์แรงหรือไม่สามารถช่วยคุณแยกแยะความแตกต่างระหว่างพันธะเคมีชนิดต่าง ๆ ที่ประกอบขึ้นเป็นสารประกอบและโมเลกุล อิเล็กโทรไลต์ที่แข็งแกร่งเป็นสารประกอบที่แยกตัวออกเป็นไอออนบวกบวกและประจุลบเชิงลบเข้าสู่สารละลายอย่างสมบูรณ์ มันดำเนินการไฟฟ้าได้ดีในการแก้ปัญหา สารประกอบอาจเป็นอิเล็กโทรไลต์ที่แรงหรืออ่อน มันเป็นสิ่งสำคัญที่จะสามารถแยกแยะความแตกต่างระหว่างคนทั้งสองเพราะแต่ละคนมีคุณสมบัติที่แตกต่างกัน
คำสั่ง
-
ตรวจสอบว่าสารประกอบเป็นอิออนหรือโควาเลนต์ สารประกอบไอออนิกโดยทั่วไปจะประกอบด้วยโลหะและอโลหะ โลหะยกเว้นไฮโดรเจนตั้งอยู่ทางด้านซ้ายของตารางธาตุในขณะที่อเมทิสตั้งอยู่ทางด้านขวา ตัวอย่างของสารประกอบไอออนิกคือ KCl หรือที่เรียกว่าโพแทสเซียมคลอไรด์ สารประกอบโควาเลนต์มักประกอบด้วยอเมทิส ตัวอย่างคือ C2H6 หรือที่เรียกว่าอีเธน หากสารประกอบนั้นเป็นโควาเลนต์ก็อาจจะไม่ใช่อิเล็กโทรไลต์ที่แรง สารประกอบของไอออนมีแนวโน้มว่าจะเป็นอิเล็กโทรไลต์ที่แข็งแรง
-
วิเคราะห์ว่าสารประกอบนั้นเป็นกรดแก่หรือไม่เพราะเป็นอิเล็กโทรไลต์ที่รุนแรง สารประกอบที่เกิดจากองค์ประกอบจากกลุ่ม 17 ของตารางเช่น HCl, HBr และ HI เป็นกรดแก่ ประเภทที่แข็งแกร่งอื่น ๆ ได้แก่ H2SO4, HNO3, HClO3 และ HClO4
-
ตรวจสอบว่าสารประกอบนั้นเป็นฐานที่แข็งแกร่งหรือไม่เนื่องจากเป็นอิเล็กโทรไลต์ที่แข็งแกร่ง สารประกอบที่เกิดขึ้นจากไฮดรอกไซด์อิออนคือฐานที่แข็งแกร่ง ตัวอย่างของสารประกอบดังกล่าว ได้แก่ LiOH, NaOH, KOH, Ca (OH) 2 และ Ba (OH) 2
-
ตรวจสอบว่าสารประกอบเกิดจากการรวมกันขององค์ประกอบกลุ่ม 1 หรือ 2 กับองค์ประกอบกลุ่ม 17 สารประกอบเหล่านี้มักจะเป็นเกลือไอออนิกซึ่งเป็นอิเล็กโทรไลต์ที่แข็งแกร่งเช่นกัน ตัวอย่างบางส่วนคือ NaCl และ KCl
-
ตกแต่งอิเล็กโทรไลต์ที่แข็งแกร่งที่สุดที่เกิดขึ้นกับสังกะสีและทองแดง สารประกอบสองชนิดที่มีอิเล็กโทรไลต์แรงคือสารประกอบไอออนิก ZnSO4 และ CuSO4 ถ้าสารประกอบใด ๆ เหล่านี้แสดงว่าเป็นอิเล็กโทรไลต์ที่แรง
สิ่งที่คุณต้องการ
- ตารางธาตุ
- คอมพิวเตอร์
- หนังสือเคมี