เนื้อหา

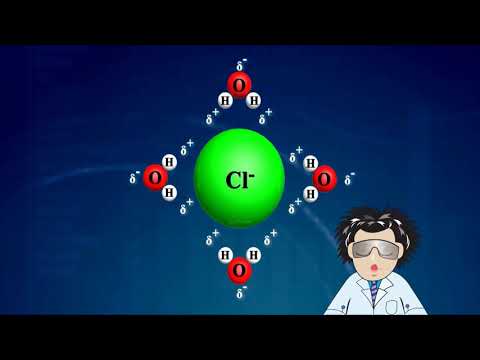
การค้นหาว่าสารประกอบเป็นอิเล็กโทรไลต์ที่แข็งแกร่งสามารถช่วยให้คุณแยกความแตกต่างระหว่างพันธะเคมีประเภทต่างๆที่ประกอบเป็นสารประกอบและโมเลกุลได้หรือไม่ อิเล็กโทรไลต์ที่แข็งแกร่งคือสารประกอบที่แยกตัวออกเป็นไอออนบวกและแอนไอออนลบในสารละลาย นำไฟฟ้าได้ดีในสารละลาย สารประกอบอาจเป็นอิเล็กโทรไลต์ที่แข็งแกร่งหรืออ่อนแอ สิ่งสำคัญคือต้องสามารถแยกความแตกต่างระหว่างทั้งสองเนื่องจากแต่ละอย่างมีคุณสมบัติที่แตกต่างกัน
ขั้นตอนที่ 1
ตรวจสอบว่าสารประกอบนั้นเป็นไอออนิกหรือโควาเลนต์ โดยทั่วไปสารประกอบไอออนิกประกอบด้วยโลหะและอโลหะ โลหะยกเว้นไฮโดรเจนจะอยู่ทางด้านซ้ายของตารางธาตุในขณะที่อเมทัลอยู่ทางด้านขวา ตัวอย่างของสารประกอบไอออนิกคือ KCl หรือที่เรียกว่าโพแทสเซียมคลอไรด์ โดยทั่วไปสารประกอบโควาเลนต์ประกอบด้วยอะเมทัล ตัวอย่างหนึ่งคือ C2H6 หรือที่เรียกว่าอีเทน ถ้าสารประกอบนั้นเป็นโควาเลนต์แสดงว่าอาจไม่ใช่อิเล็กโทรไลต์ที่แรง สารประกอบไอออนิกมีแนวโน้มที่จะเป็นอิเล็กโทรไลต์ที่แข็งแกร่ง
ขั้นตอนที่ 2
วิเคราะห์ว่าสารประกอบนั้นเป็นกรดแก่หรือไม่เนื่องจากเป็นอิเล็กโทรไลต์ที่เข้มข้น สารประกอบที่เกิดจากองค์ประกอบของกลุ่ม 17 ของตารางเช่น HCl, HBr และ HI เป็นกรดแก่ ประเภทอื่น ๆ ที่แข็งแกร่ง ได้แก่ H2SO4, HNO3, HClO3 และ HClO4
ขั้นตอนที่ 3
ตรวจสอบว่าสารประกอบนั้นมีความแข็งแรงหรือไม่เนื่องจากเป็นอิเล็กโทรไลต์ที่แข็งแกร่ง สารประกอบที่เกิดจากไฮดรอกไซด์ไอออน OH- เป็นเบสที่แข็งแกร่ง ตัวอย่างบางส่วนของสารประกอบเหล่านี้ ได้แก่ LiOH, NaOH, KOH, Ca (OH) 2 และ Ba (OH) 2
ขั้นตอนที่ 4
ตรวจสอบว่าสารประกอบเกิดจากการรวมกันของธาตุกลุ่ม 1 หรือ 2 กับธาตุกลุ่ม 17 โดยปกติสารประกอบเหล่านี้เป็นเกลือไอออนิกซึ่งเป็นอิเล็กโทรไลต์ที่เข้มข้นเช่นกัน ตัวอย่างบางส่วน ได้แก่ NaCl และ KCl
ขั้นตอนที่ 5
ตกแต่งอิเล็กโทรไลต์ที่แข็งแกร่งที่สุดซึ่งขึ้นรูปด้วยสังกะสีและทองแดง สารประกอบสองชนิดที่เป็นอิเล็กโทรไลต์ที่แข็งแกร่งคือสารประกอบไอออนิก ZnSO4 และ CuSO4 ถ้าสารประกอบเหล่านี้เป็นอิเล็กโทรไลต์ที่แข็งแกร่งอย่างแน่นอน